珈創(chuàng)生物 —— 生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè)
優(yōu)質(zhì)高效透明
High quality, efficient and transparent
發(fā)布時間:2022-12-05 16:32 信息來源: 閱讀次數(shù): 次
來源于人或動物細胞系的生物技術(shù)產(chǎn)品的一個共同特點是存在病毒污染的風(fēng)險,污染可來自原細胞系(細胞基質(zhì))本身,也可來自生產(chǎn)過程中偶然帶入的外源病毒,這種污染可能產(chǎn)生嚴(yán)重的臨床后果。
風(fēng)險控制原則
控制生物技術(shù)產(chǎn)品的潛在病毒污染,可歸納為以下三條相互補充的原則:
a)選擇并對選定的細胞系和其他原料進行檢定,確保其不含可能對人有感染和/或致病作用的病毒。
b)評估生產(chǎn)工藝清除感染性病毒的能力。
c)檢測生產(chǎn)適當(dāng)步驟的產(chǎn)品,確保產(chǎn)品未受感染性病毒的污染。
各級細胞病毒安全性控制
細胞庫包括原始細胞庫(PCB,又稱細胞種子)、主細胞庫(MCB)和工作細胞庫(WCB)。
ICH Q5A(R1)及USP-NF<1050>中對不同級別細胞進行病毒檢測的建議:
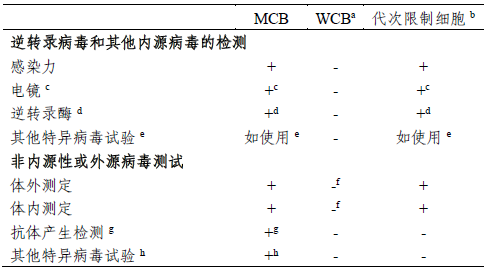
a.作為藥物生產(chǎn)起始細胞基質(zhì)的工作細胞庫,必須進行外源病毒檢測,既可對WCB進行直接測定,也可對從WCB來源的體外傳代限度內(nèi)的細胞進行分析。
b. 達到限傳代次的細胞:在體外達到傳代限度的生產(chǎn)細胞。
c. 也可測定其他因子。
d. 若逆轉(zhuǎn)錄病毒感染試驗為陽性,則無須檢測。
e. 指使用于已受此因子感染的細胞系。
f. 對第一個WCB,此測試應(yīng)在該WCB產(chǎn)生的達到體外限傳代次細胞上進行;以后的WCB,可直接在WCB上進行單項體外和體內(nèi)測試,或在達到體外限傳代次的細胞上測試。
g. 例如,MAP、RAP、HAP-通常適用于嚙齒細胞系。
h. 例如,適用于人、非人靈長目或其他細胞的測試方法。
EP10.0 <5.2.3>中對不同級別細胞系進行病毒檢測的建議:
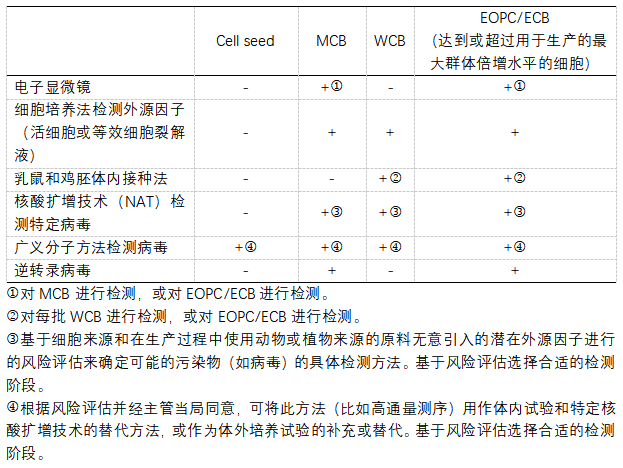
中國藥典三部(2020版)對細胞基質(zhì)及細胞庫體系的病毒檢查的建議:
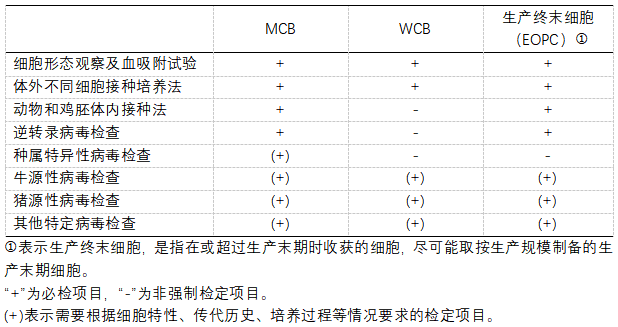
通過以上法規(guī)要求可以看出,對于細胞基質(zhì)和各級細胞庫,具體的檢定項目需要根據(jù)特定的細胞特性、傳代歷史、培養(yǎng)過程、生產(chǎn)工藝等進行綜合評估。根據(jù)ICH Q5A的要求,應(yīng)對MCB進行內(nèi)源性和非內(nèi)源性病毒污染的檢測;如果不檢測MCB,也可以使用WCB全面檢測進行替代。
生產(chǎn)過程中感染性病毒污染的風(fēng)險控制
雖然在細胞庫階段對MCB 和WCB 進行了內(nèi)外源病毒因子檢測,但有些內(nèi)源性病毒可能在MCB 和WCB 階段未被檢出,或者在生產(chǎn)過程中引入偶然的病毒因子污染,因而對生產(chǎn)終末細胞和/或細胞收獲液中的病毒因子進行檢測和控制非常重要。
對于UPB樣品,ICH Q5A僅要求在進行上市注冊申請時,至少應(yīng)上報三批試生產(chǎn)或規(guī)模化生產(chǎn)的UPB研究資料,一般使用一種或幾種細胞系進行體外篩查試驗。如適用,可使用PCR試驗或其他適當(dāng)?shù)姆椒āMA文件《Guideline on Virus Safety Evaluation of Biotechnological Investigational Products》則指出,每一批用于臨床試驗的UPB均應(yīng)按照ICH Q5A的要求進行檢測,具體不同細胞系對應(yīng)的檢測方法也有不同。
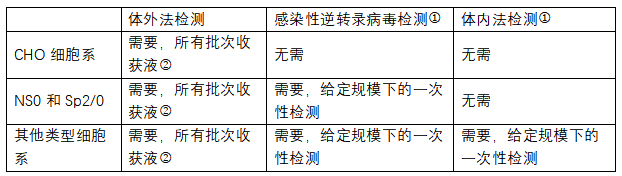
①如果可能,檢測樣品應(yīng)包括細胞或細胞碎片以進行細胞相關(guān)病毒檢測。對于灌注式細胞培養(yǎng),生產(chǎn)商應(yīng)確定并證明最適合的樣品(含細胞的樣品)收集步驟,收集超出批量生產(chǎn)代次的細胞檢測樣品也是可行的;在上述情況下,應(yīng)證明采用分析方法的合理性;如果已有敏感度更高的方法可表明感染逆轉(zhuǎn)錄病毒檢測結(jié)果為陰性,則感染性逆轉(zhuǎn)錄病毒的檢測可忽略。②僅需在研發(fā)的特定階段對前三批原液進行逆轉(zhuǎn)錄病毒或逆轉(zhuǎn)錄病毒顆粒的檢測(如果制備批次不足三批,也可用更少批次)。
FDA指導(dǎo)文件《Points to Consider in the Manufacture and Testing of Monoclonal Antibody Products for Human Use》中則對UPB、純化中間品和成品的病毒檢測都有不同要求。對于每個批次收獲液需要進行外源病毒因子、種屬特異性病毒、逆轉(zhuǎn)錄病毒或逆轉(zhuǎn)錄病毒顆粒定量的檢測。
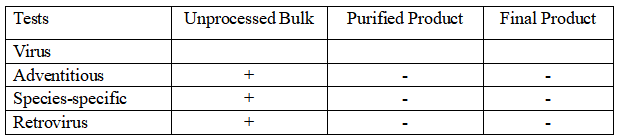
根據(jù)中國藥典三部(2020版)要求對于人用生物制品生產(chǎn)用動物細胞基質(zhì)及檢定用動物細胞,需要對MCB進行全面檢定,并且需要對EOPC進行檢定。對于人用重組單克隆抗體制品生產(chǎn),應(yīng)根據(jù)生產(chǎn)過程及所用材料的特點,在合適的階段進行常規(guī)或特定的外源病毒污染檢查。除另有規(guī)定外,應(yīng)對限定細胞傳代次數(shù)的生產(chǎn)方式,采用適當(dāng)?shù)捏w外方法至少對3次收獲物進行外源病毒檢測。
相關(guān)法規(guī)指導(dǎo)
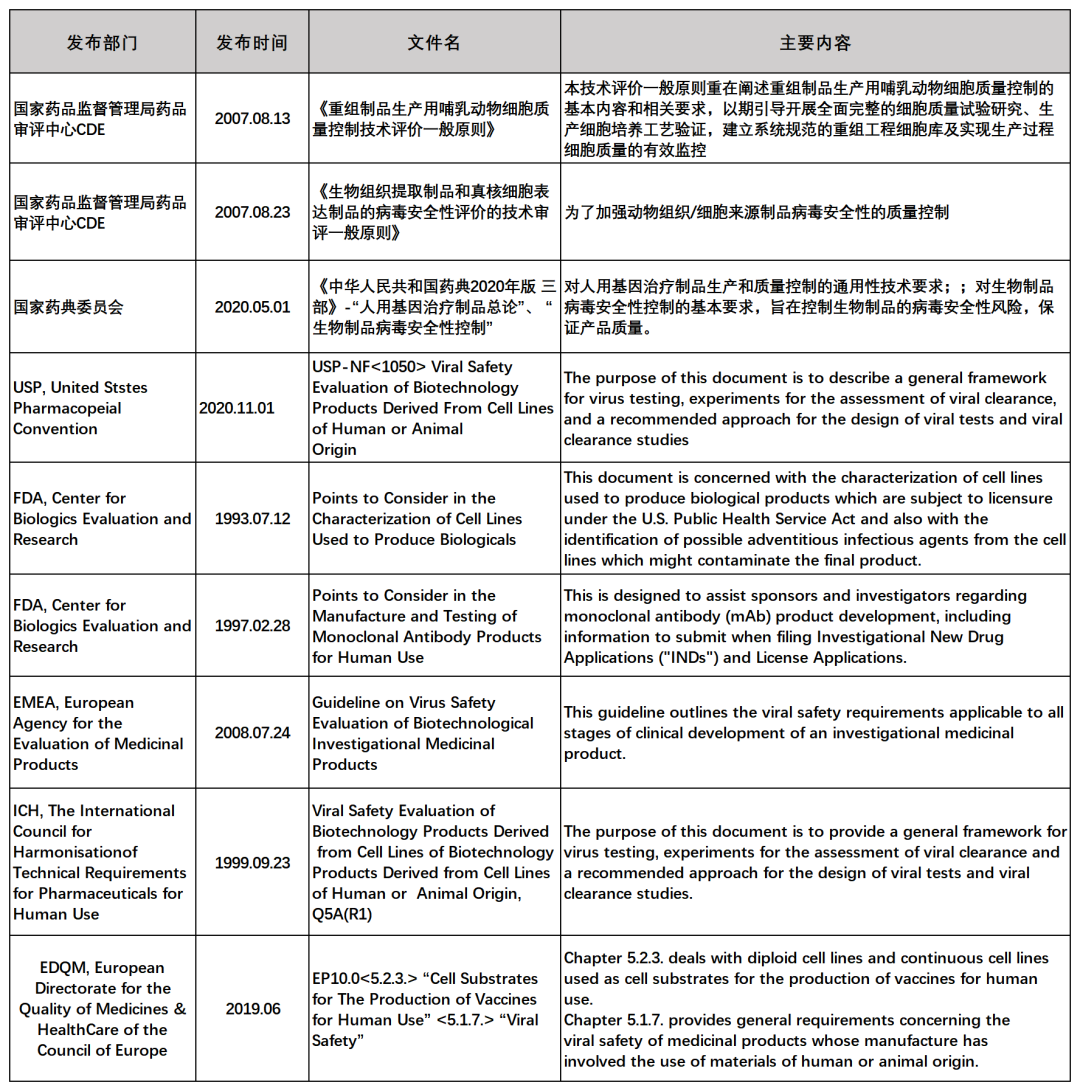
近年來,雖然對于內(nèi)外源病毒因子檢測中外申報要求各異,但2020年1月NMPA發(fā)布的“國家藥監(jiān)局關(guān)于適用《Q2(R1):分析方法論證:正文和方法學(xué)》等11個國際人用藥品注冊技術(shù)協(xié)調(diào)會指導(dǎo)原則的公告(2020年第7號)”中包含ICH Q5A(R1)和Q5B等文件,這表明國內(nèi)法規(guī)正逐漸與國際相關(guān)法規(guī)接軌,給國內(nèi)制藥企業(yè)進行中外雙報帶來了便利,從而加速藥品上市。
后臺回復(fù)“病毒檢測指導(dǎo)”,獲取相關(guān)指導(dǎo)文件。
武漢珈創(chuàng)生物相關(guān)服務(wù)
武漢珈創(chuàng)生物技術(shù)股份有限公司,創(chuàng)建于2011年,是一家集生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè),專注于為生物藥品/制品的生產(chǎn)企業(yè)及研發(fā)機構(gòu)提供各類細胞(含重組細胞、干細胞、免疫細胞等)及原輔料的質(zhì)量檢測、病毒清除工藝驗證技術(shù)服務(wù)。
質(zhì)量檢測服務(wù)
武漢珈創(chuàng)生物可按相關(guān)法規(guī)或指導(dǎo)原則提供各類細胞基質(zhì)的成瘤性檢查服務(wù),且有多種檢測方法可供選擇如動物體內(nèi)接種法(裸鼠)、軟瓊脂克隆形成試驗、端粒酶活性檢測等,至今已完成數(shù)萬批次的細胞及產(chǎn)品檢測服務(wù)。
定制化服務(wù)
針對特殊需求,我們還可提供定制化的檢測服務(wù),歡迎新老客戶前來咨詢。

END