珈創(chuàng)生物 —— 生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè)
優(yōu)質(zhì)高效透明
High quality, efficient and transparent
發(fā)布時間:2022-11-23 15:49 信息來源: 閱讀次數(shù): 次
自1992年,美國生物學(xué)家Arnold Caplan教授命名 “間充質(zhì)干細胞”并開啟了世界上第一例間充質(zhì)干細胞的臨床探索至今,人類探索干細胞臨床應(yīng)用的歷史已三十余年。干細胞是一類具有不同分化潛能,并能在非分化狀態(tài)下自我更新的細胞。常用于細胞治療的干細胞一般可分為胚胎干細胞、成體干細胞(如脂肪間充質(zhì)干細胞、骨髓間充質(zhì)干細胞、臍帶間充質(zhì)干細胞等)、誘導(dǎo)多能干細胞。
干細胞治療是指應(yīng)用人自體或異體來源的干細胞,經(jīng)體外操作后輸入(或植入)人體,用于疾病治療。這種體外操作包括干細胞的分離、純化、擴增、修飾、干細胞(系)的建立、誘導(dǎo)分化、凍存和凍存后的復(fù)蘇等過程。
研究近況
目前在clinicaltrials.gov網(wǎng)站上已登記的干細胞臨床研究項目超過1W個,10多款產(chǎn)品在各國已獲批上市,大部分已獲批上市的產(chǎn)品主要是根據(jù)其免疫調(diào)控和組織修復(fù)兩個生物學(xué)特性應(yīng)用于相應(yīng)適應(yīng)癥,如移植物抗宿主病、膝骨關(guān)節(jié)炎、克羅恩病,嚴重肢體缺血等。
干細胞產(chǎn)品工藝簡介
干細胞制劑的制備工藝包括干細胞的采集、分離、純化、擴增和傳代,干細胞(系)的建立、向功能性細胞定向分化,培養(yǎng)基、輔料和包材的選擇標準及使用,細胞凍存、復(fù)蘇、分裝和標記,以及殘余物去除等。
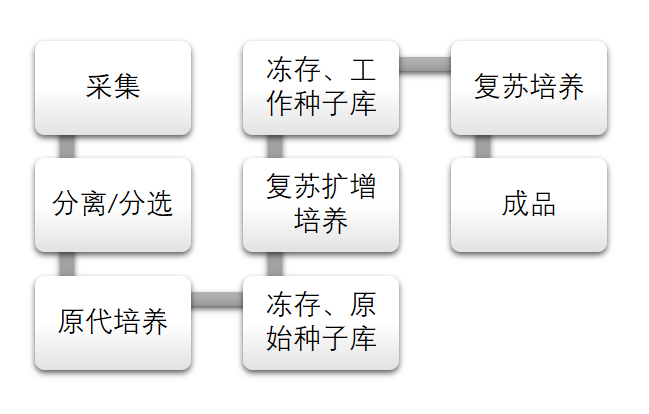
干細胞產(chǎn)品工藝流程▲
點擊看大圖
“類雙軌制”監(jiān)管模式
在我國,干細胞治療產(chǎn)品目前處在“類雙軌制”的監(jiān)管階段。按照“藥品監(jiān)管”,該類監(jiān)管是指由企業(yè)通過注冊IND并完成三期臨床試驗,最后作為藥品上市銷售;按照“醫(yī)療技術(shù)監(jiān)管”,該類監(jiān)管是指根據(jù)衛(wèi)健委和藥監(jiān)局出臺的《干細胞臨床研究管理辦法》,通過兩委局的備案以后,開展研究者發(fā)起的干細胞臨床研究。無論何種途徑,其向臨床轉(zhuǎn)化的過程都必須遵守相關(guān)規(guī)定,嚴格執(zhí)行行業(yè)標準。
隨著細胞治療產(chǎn)品的蓬勃發(fā)展和相應(yīng)法規(guī)及技術(shù)指南的不斷完善,干細胞臨床研究和轉(zhuǎn)化以按“藥品管理”為主的趨勢正逐漸明朗,研究者從早期的研究階段開始,就必須考慮到作為藥物研發(fā)亦或是臨床研究備案時的方方面面,以提高轉(zhuǎn)化效率。
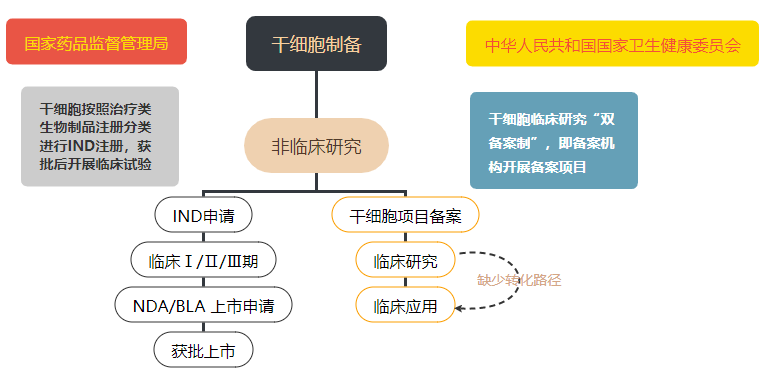
干細胞監(jiān)管模式▲
點擊看大圖
相關(guān)法規(guī)指導(dǎo)要點
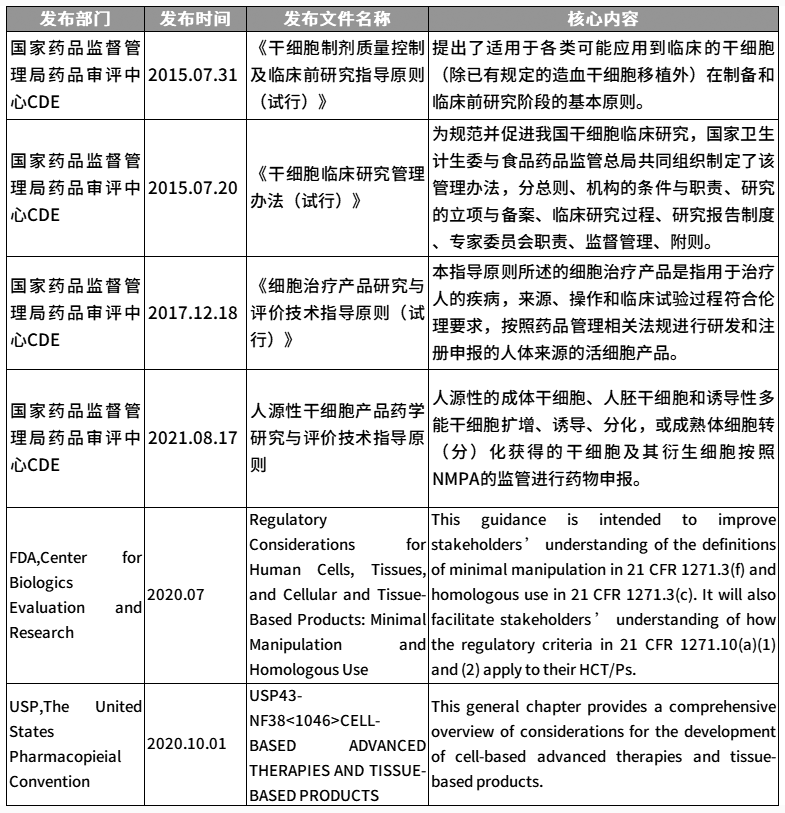
干細胞法規(guī)文件▲
點擊看大圖
回復(fù)“干細胞質(zhì)量控制”,獲取相關(guān)法規(guī)文件原件
根據(jù)相應(yīng)法規(guī)和指導(dǎo)文件,對生產(chǎn)過程中的使用材料、生產(chǎn)工藝和過程控制、質(zhì)量研究和控制、穩(wěn)定性研究等的基本要求匯總?cè)缦拢?
01
相關(guān)依據(jù)
干細胞臨床研究應(yīng)當符合《藥物臨床試驗質(zhì)量管理規(guī)范》的要求;干細胞制劑符合《干細胞制劑質(zhì)量控制及臨床前研究指導(dǎo)原則(試行)》的要求;干細胞制劑的制備應(yīng)當符合《藥品生產(chǎn)質(zhì)量管理規(guī)范》(GMP)的基本原則和相關(guān)要求。
02
全過程質(zhì)量控制
所有干細胞制劑都可遵循一個共同的研發(fā)過程,即從干細胞制劑的制備、體外試驗、體內(nèi)動物試驗,到植入人體的臨床研究及臨床治療的過程。整個過程的每一階段,都須對所使用的干細胞制劑在細胞質(zhì)量、安全性和生物學(xué)效應(yīng)方面進行相關(guān)的研究和質(zhì)量控制。干細胞生產(chǎn)過程中的每一個生產(chǎn)步驟均應(yīng)該進行研究與驗證,并根據(jù)工藝特點設(shè)置重要工藝步驟的監(jiān)控點,加強監(jiān)控。
03
原材料控制
干細胞產(chǎn)品生產(chǎn)用的生物材料,如細胞株、培養(yǎng)基、滋養(yǎng)層細胞、動物來源的試劑和血清等,企業(yè)應(yīng)當保證其來源合法、安全并符合質(zhì)量標準,防止引入或傳播傳染病病原體。
04
產(chǎn)品檢測
干細胞產(chǎn)品的檢測機制建議采用質(zhì)量檢驗和放行檢驗與專業(yè)檢測機構(gòu)復(fù)核檢測相結(jié)合的方法,即這種“質(zhì)量檢驗” -“放行檢驗” -“復(fù)核檢驗”的評價體系。
質(zhì)量檢驗
為保證干細胞經(jīng)特定體外處理后的安全性、有效性和質(zhì)量可控性而進行的較全面質(zhì)量檢驗。須對多批次干細胞制劑進行質(zhì)量檢驗,檢定項目應(yīng)當建立在產(chǎn)品質(zhì)量研究以及對生產(chǎn)工藝和生產(chǎn)過程充分理解的基礎(chǔ)之上,同時兼顧產(chǎn)品的特性和當下的科學(xué)認知與共識。
放行檢驗
在完成質(zhì)量檢驗的基礎(chǔ)上,對每一類型的每一批次干細胞制劑,在臨床應(yīng)用前所應(yīng)進行的相對快速和簡化的細胞檢驗。可建立針對不同階段關(guān)鍵制備工藝的過程控制,和針對不同組織來源批次及生產(chǎn)制備批次的中間細胞形態(tài)和終末制劑標準放行的評價規(guī)范。
質(zhì)量復(fù)核
由專業(yè)細胞檢驗機構(gòu)/實驗室進行干細胞制劑的質(zhì)量復(fù)核檢驗,并出具檢驗報告。
05
質(zhì)量研究
干細胞產(chǎn)品的質(zhì)量研究應(yīng)選擇有代表性的生產(chǎn)批次和合適的生產(chǎn)階段樣品(如初始分離的細胞、制備過程中細胞或成品等)進行研究。質(zhì)量研究應(yīng)涵蓋細胞特性分析、功能性分析、純度分析和安全性分析等方面,并且根據(jù)產(chǎn)品的自身特性可再增加其他相關(guān)的研究項目。
風(fēng)險評估與控制
除了一般生物制品的常見風(fēng)險外,干細胞產(chǎn)品的風(fēng)險還包括污染和交叉污染的風(fēng)險(供者、原材料、操作過程)、 高風(fēng)險起始原材料(ESCs/iPSCs、基因遞送與修飾系統(tǒng))殘留的風(fēng)險、 加工過程中非目的細胞、非預(yù)期變化等雜質(zhì)的風(fēng)險、生產(chǎn)工藝變更的風(fēng)險和干細胞產(chǎn)品的其他質(zhì)量風(fēng)險因素。
研發(fā)者應(yīng)在綜合考慮各種因素的基礎(chǔ)上,針對不同類型產(chǎn)品特性和全生命周期過程評估產(chǎn)品的總體風(fēng)險,并制定相應(yīng)的風(fēng)險控制策略。
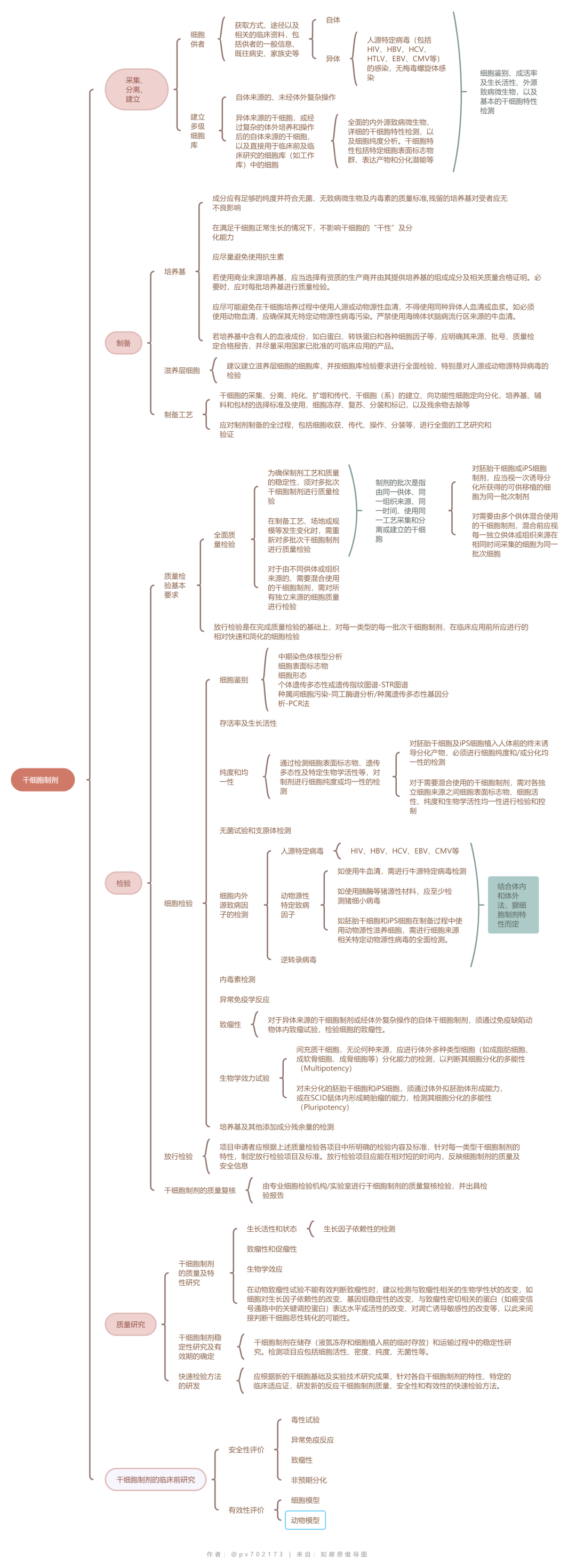
干細胞質(zhì)量控制▲
點擊看大圖
武漢珈創(chuàng)生物相關(guān)服務(wù)
武漢珈創(chuàng)生物技術(shù)股份有限公司,創(chuàng)建于2011年,是一家集生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè),專注于為生物藥品/制品的生產(chǎn)企業(yè)及研發(fā)機構(gòu)提供各類細胞(含重組細胞、干細胞、免疫細胞等)及原輔料的質(zhì)量檢測、病毒清除工藝驗證技術(shù)服務(wù)。
質(zhì)量檢測服務(wù)
武漢珈創(chuàng)生物可按相關(guān)法規(guī)或者指導(dǎo)文件提供干細胞治療產(chǎn)品的各個生產(chǎn)環(huán)節(jié)的質(zhì)量檢測服務(wù),包括:
基本生物學(xué)屬性檢測
細胞鑒別、細胞活性檢測、種屬間細胞污染的檢測、染色體核型分析;
微生物學(xué)安全性檢測
無菌檢測、支原體檢測,確保產(chǎn)品無微生物污染或代謝產(chǎn)物污染;
生物學(xué)安全性檢測
成瘤性和致瘤性檢測、異常免疫反應(yīng)檢測、殘留物的檢測;
生物學(xué)有效性評價
多向分化功能的評價、免疫調(diào)控功能的評價、hMSCs組織再生功能的評價
干細胞放行快檢
珈創(chuàng)生物自主研發(fā)的放行快檢技術(shù),可在6小時內(nèi)完成,涵蓋細菌、真菌和支原體快檢技術(shù),且技術(shù)方法已成熟,經(jīng)過了上百次驗證。
定制化服務(wù)
針對特殊需求,我們還可提供定制化的檢測服務(wù),歡迎新老客戶前來咨詢。
參考資料:
[1]周萍,李昂,李欣,陸東哲,王曉熙,吳朝暉,薛迪.干細胞研究與臨床應(yīng)用的倫理規(guī)范與監(jiān)管[J/OL].上海預(yù)防醫(yī)學(xué):1-5[2022-11-02].http://kns.cnki.net/kcms/detail/31.1635.R.20220721.1739.013.html
[2]王晶,黃云虹,高晨燕.我國間充質(zhì)干細胞產(chǎn)品的注冊申請情況及臨床審評中的幾點考慮[J].中國新藥雜志,2022,31(15):1468-1473.
[3]一文覽盡:中國干細胞藥物注冊申報和受理
https://mp.weixin.qq.com/s/PhoTzjxpVmGwahQe2K4nqw
[4]張可華,納濤,韓曉燕,吳婷婷,張麗霞,賈春翠,袁翔鶴,馮建萍,項楠,孟淑芳.干細胞臨床研究質(zhì)量復(fù)核中發(fā)現(xiàn)的問題及初步分析[J].中國新藥雜志,2021,30(19):1746-1751.

END