珈創(chuàng)生物 —— 生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè)
優(yōu)質(zhì)高效透明
High quality, efficient and transparent
發(fā)布時間:2022-09-15 17:15 信息來源: 閱讀次數(shù): 次
武漢珈創(chuàng)生物祝賀合作伙伴安徽中盛溯源、康希諾、百奧泰近日喜獲審批,祝愿他們再創(chuàng)新高!
接下來,珈創(chuàng)小助手將帶你回顧近期行業(yè)申報熱點資訊,了解行業(yè)動態(tài)。
近期行業(yè)重磅申報審批盤點
▼
01
2022年9月8日,據(jù)CDE官網(wǎng)顯示,安徽中盛溯源生物科技有限公司(下面簡稱“中盛溯源”)的“NCR100注射液”獲批臨床,擬開展針對膝骨關(guān)節(jié)炎的臨床試驗。根據(jù)中盛溯源官網(wǎng),該藥物應(yīng)該為一款iPSC來源的細胞治療藥物。

干細胞療法作為一種突破性的治療方法,可以在一定的條件下將干細胞誘導(dǎo)分化成軟骨細胞或者成骨細胞,經(jīng)過增殖生成大量的高質(zhì)量的軟骨細胞后注入到人體當(dāng)中。進而對那些出現(xiàn)損傷的軟骨器官進行修復(fù),達到治愈膝骨關(guān)節(jié)炎的效果。
02
近日,康希諾生物股份公司吸入用重組新型冠狀病毒疫苗(5型腺病毒載體)克威莎®(Convidecia)霧優(yōu)®,已通過國家藥品監(jiān)督管理局組織論證同意作為加強針納入緊急使用。
克威莎®霧優(yōu)®在肌注型腺病毒載體新冠疫苗克威莎®的基礎(chǔ)上創(chuàng)新給藥方式,用霧化器將疫苗霧化成微小顆粒,通過口腔吸入的方式完成接種。該接種過程無需針刺,一呼一吸間即可獲得高效免疫保護
03
百奧泰生物制藥股份有限公司(證券代碼:688177)最近收到國家藥品監(jiān)督管理局核準簽發(fā)的關(guān)于公司在研產(chǎn)品注射用 BAT8008 的《臨床試驗批準通知書》。
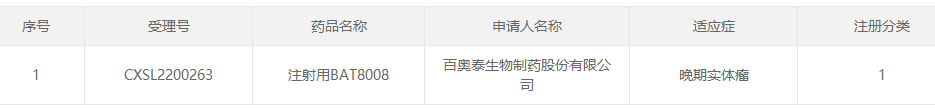
BAT8008 是百奧泰開發(fā)的靶向 Trop2 的抗體藥物偶聯(lián)物(ADC),擬開發(fā)用于實體腫瘤治療。Trop-2(Trophoblast cell-surface antigens 2,Trop2),又稱為TACSTD2、M1S1、GA733-1、EGP-1),是腫瘤相關(guān)鈣信號轉(zhuǎn)導(dǎo)蛋白(Tumor associated calcium signal transducer,TACSTD)基因家族的一員,與細胞內(nèi)鈣離子濃度的調(diào)控有關(guān)。
Trop2在正常人體組織中不表達或低表達,高表達于多種類型的人類腫瘤組織,該差異使得 Trop2 成為 ADC 藥物的熱門靶點。BAT8008 由重組人源化抗 Trop2 抗體與毒性小分子拓撲異構(gòu)酶 I 抑制劑通過自主研發(fā)的可剪切連接子連接而成。BAT8008 具有高效的抗腫瘤活性,毒素小分子有較強的旁觀者效應(yīng),可有效克服腫瘤組織的異質(zhì)性。同時,BAT8008 具有較好的穩(wěn)定性及安全性,血漿中釋放的毒素小分子極低,降低了脫靶毒性的風(fēng)險。
04
近日,細胞療法公司Immusoft宣布,F(xiàn)DA已批準其工程化B細胞療法ISP-001用于治療MPSI(I型粘多糖貯積癥)的IND申請。ISP-001是一種基于Immusoft的免疫系統(tǒng)編程(ISP?),能避免與病毒傳遞相關(guān)的免疫原性和化療預(yù)處理并且可持續(xù)進行治療性蛋白質(zhì)遞送的工程化B細胞療法,該藥物已獲得FDA孤兒藥物指定并將于今年啟動1期研究。如果進展順利,ISP-001將成為首個進入臨床試驗的工程化B細胞療法。
該療法可對患者的B細胞進行重新編程,以持續(xù)生產(chǎn)治療性蛋白質(zhì),從而減少頻繁輸注的需要,并改善患者的預(yù)后
05
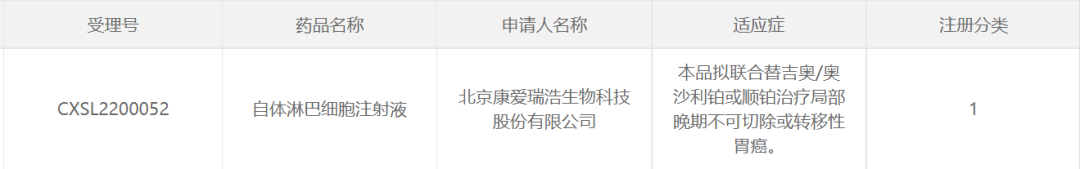
近期,國家藥監(jiān)局藥品審評中心(CDE)官網(wǎng)顯示,北京康愛瑞浩生物科技股份有限公司(以下簡稱:康愛生物)自主研發(fā)的KACM001自體淋巴細胞注射液產(chǎn)品正式獲得臨床試驗?zāi)驹S可,擬聯(lián)合替吉奧/奧沙利鉑或順鉑治療局部晚期不可切除或轉(zhuǎn)移性胃癌。是目前國內(nèi)首個聯(lián)合一線治療方案,針對實體腫瘤的1類新藥。同時,KACM001在其他實體腫瘤治療中同樣展現(xiàn)了明顯的安全和有效性,未來有望成為新一代廣譜抗腫瘤藥物。
MTCA-CTL免疫療法是國內(nèi)推出的新一代生物免疫治療模式。在保證非MHC(主要組織相容性復(fù)合體)限制性殺傷性NK-T細胞擴增的同時,定向擴增HC限制性的CD8+特異性CTL細胞(細胞毒性T淋巴細胞),使其在細胞產(chǎn)品中的比率可達到60%~70%。這種殺傷細胞的共同作用,使殺傷腫瘤細胞的效率更高。
06
8月17日,藍鳥生物宣布美國FDA批準Zynteglo用于治療β地中海貧血。這是第一個針對需要定期輸血的 β地中海貧血患者的基因療法。據(jù)了解,藍鳥生物為Zynteglo的定價為280萬美元,超過諾華的基因療法Zolgensma(定價210萬美元),一躍成為“史上最貴藥”。
該療法是一種定制設(shè)計的一種一次性基因療法,它通過將β-珠蛋白基因的修飾形式的功能拷貝添加到患者自身的造血干細胞中來發(fā)揮作用。
07
8月11日,阿斯利康(AstraZeneca)和第一三共制藥( Daiichi Sankyo)共同研發(fā)的乳腺癌藥物 Enhertu(德喜曲妥珠單抗,簡稱T-DXd,DS-8201)獲批新適應(yīng)癥,成為首款治療非小細胞肺癌的HER2靶向藥。
紀念斯隆-凱特琳癌癥中心的Bob T. Li博士表示:“這是肺癌治療的一個重要里程碑。經(jīng)過二十年的研究之后,首個 HER2 靶向治療方案的批準證實了 HER2 基因是肺癌靶向治療的重要靶點,并標志著在治療NSCLC方面向前邁出了重要一步。”
08
8月31日,美國食品藥品監(jiān)督管理局(FDA)批準Moderna、輝瑞/BioNTech針對奧密克戎變異株 BA.4/BA.5的二價新冠mRNA疫苗的緊急使用授權(quán)(EUAs)申請,授權(quán)兩家公司的二價mRNA疫苗作為單劑加強針,在完成接種基礎(chǔ)劑量疫苗,或者在最新一劑加強針至少兩個月后,方可接種。該款從研發(fā)到獲批,僅用了60余天。

09
近日(2022年9月2日),勃林格殷格翰宣布,F(xiàn)DA批準IL-36R單抗spesolimab上市,用于治療泛發(fā)性膿皰型銀屑病(GPP)發(fā)作,商品名為Spevigo。Spesolimab治療GPP適應(yīng)上市申請已獲EMA受理,并于今年3月被CDE納入優(yōu)先審評。
spesolimab是一款first-in-class靶向IL-36單抗,可阻斷白細胞介素-36受體(IL-36R)作用。
10
近日,CDE官網(wǎng)公示顯示,華夏英泰(北京)生物技術(shù)有限公司(簡稱“華夏英泰”)提交的HXYT-001細胞注射液獲得一項臨床試驗?zāi)驹S可,擬開發(fā)用于治療復(fù)發(fā)/難治 B 細胞非霍奇金淋巴瘤(B-NHL), 包括彌漫大 B 細胞淋巴瘤、原發(fā)縱膈大 B 細胞淋巴瘤、濾泡性淋巴瘤轉(zhuǎn)化的彌漫大 B 細胞淋巴瘤、 濾泡性淋巴瘤 3b 級、高級別 B 細胞淋巴瘤伴 MYC 和 BCL2 和/或 BCL6 重排和高級別 B 細胞淋巴瘤-非特指型。

11
近日,CDE官網(wǎng)公示顯示,深圳市華藥康明生物藥業(yè)有限責(zé)任公司(簡稱“華藥康明”)提交的KM1溶瘤痘苗病毒注射液獲得一項臨床試驗?zāi)驹S可,擬開發(fā)用于晚期無有效治療手段的惡性實體瘤。

圖片及內(nèi)容來源于網(wǎng)絡(luò),本平臺旨在共享知識,如侵聯(lián)刪。
關(guān)于珈創(chuàng)生物
武漢珈創(chuàng)生物技術(shù)股份有限公司,創(chuàng)建于2011年,是一家集生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè),專注于為生物藥品/制品的生產(chǎn)企業(yè)及研發(fā)機構(gòu)提供各類細胞(含重組細胞、干細胞、免疫細胞等)及原輔料的質(zhì)量檢測、病毒清除工藝驗證技術(shù)服務(wù)。