珈創(chuàng)生物 —— 生物技術(shù)服務(wù)與研發(fā)為一體的高新技術(shù)企業(yè)
優(yōu)質(zhì)高效透明
High quality, efficient and transparent
發(fā)布時(shí)間:2020-01-16 09:59 信息來(lái)源: 閱讀次數(shù): 次
前言
近年來(lái),DNA 重組技術(shù)在醫(yī)藥領(lǐng)域的飛速發(fā)展,使得采用哺乳動(dòng)物細(xì)胞表達(dá)系統(tǒng)的生物制品藥物逐漸成為主流,而對(duì)于此技術(shù)的主要原材料---細(xì)胞系和其他原料的檢定要求也日趨嚴(yán)格。

隨著質(zhì)量源于設(shè)計(jì)(QbD)理念越來(lái)越廣泛的得到認(rèn)可,意味著僅僅依靠檢測(cè)終產(chǎn)品來(lái)保證藥品質(zhì)量是遠(yuǎn)遠(yuǎn)不夠的,這個(gè)理念和生物制品一直堅(jiān)持的全過(guò)程質(zhì)量控制的基本方針是基本一致的。基于這一理念,把控生產(chǎn)用細(xì)胞的構(gòu)建、鑒定,以及細(xì)胞庫(kù)的建立和管理,能夠從源頭上保證產(chǎn)品質(zhì)量的穩(wěn)定。
2015年版《中國(guó)藥典》三部“生物制品生產(chǎn)用動(dòng)物細(xì)胞制備及檢定規(guī)程”中,對(duì)于生產(chǎn)用細(xì)胞基質(zhì)的質(zhì)量控制提出了要求。對(duì)于生產(chǎn)用細(xì)胞,需要建立細(xì)胞庫(kù),細(xì)胞庫(kù)的建立可為生物制品的生產(chǎn)提供檢定合格,質(zhì)量相同,能持續(xù)穩(wěn)定傳代的細(xì)胞。在細(xì)胞庫(kù)建立之后,應(yīng)至少對(duì)MCB和生產(chǎn)終末細(xì)胞進(jìn)行一次全面檢定。當(dāng)生產(chǎn)工藝發(fā)生改變時(shí),還應(yīng)重新對(duì)生產(chǎn)終末細(xì)胞進(jìn)行全檢。細(xì)胞檢定主要包括以下幾個(gè)方面:細(xì)胞鑒別、外源因子和內(nèi)源因子的檢查、成瘤性/致瘤性檢查等。細(xì)胞檢定的基本要求見(jiàn)下表:
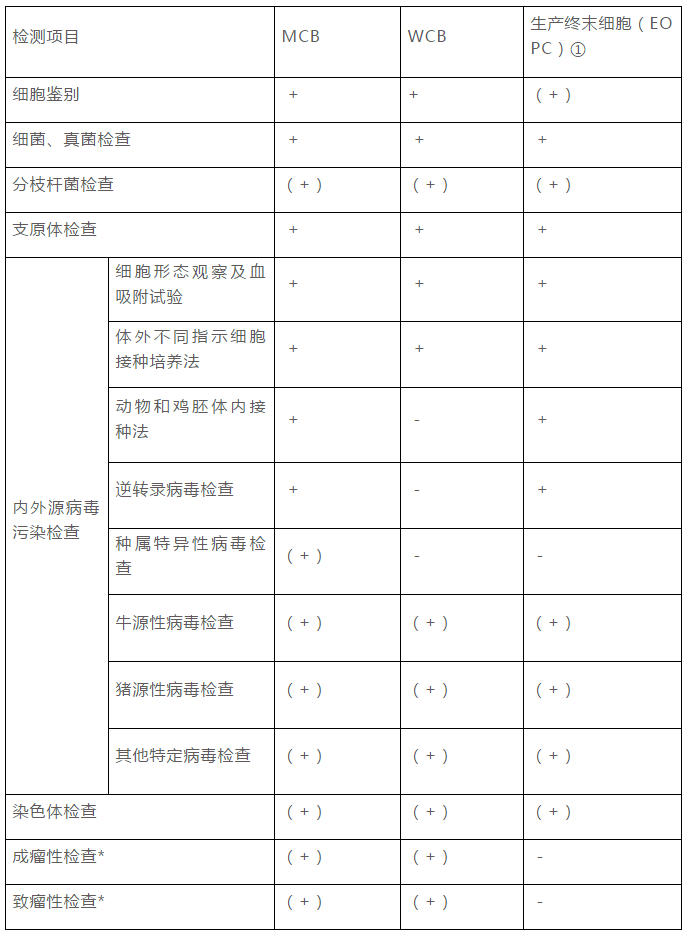

細(xì)胞庫(kù)的檢定,對(duì)于保證細(xì)胞庫(kù)的質(zhì)量和為后續(xù)工藝提供穩(wěn)定的合格的細(xì)胞尤為必要,此部分的工作對(duì)生物制品產(chǎn)品而言非常重要。在進(jìn)行項(xiàng)目選擇時(shí),可參考《中國(guó)藥典》三部“生物制品生產(chǎn)用動(dòng)物細(xì)胞制備及檢定規(guī)程”。
大多數(shù)生物制品產(chǎn)品是有活性的,無(wú)法采用傳統(tǒng)的終端滅菌工藝,因此在細(xì)胞庫(kù)建立和生產(chǎn)的各個(gè)階段都需要對(duì)無(wú)菌性進(jìn)行檢定,其中分枝桿菌的檢查是2015年版藥典新增項(xiàng)目,檢定時(shí)應(yīng)關(guān)注。
支原體的污染則是基礎(chǔ)研究和工業(yè)生產(chǎn)中的常見(jiàn)問(wèn)題,據(jù)報(bào)道可能有高達(dá)87%的細(xì)胞系發(fā)生過(guò)支原體污染,支原體在光學(xué)顯微鏡下不可見(jiàn),一般不引起培養(yǎng)物渾濁,因此支原體污染一般很難察覺(jué),支原體檢測(cè)也十分必要。
感染性病毒顆粒污染生物制品和生物制品衍生產(chǎn)品是被廣泛關(guān)注的安全問(wèn)題,對(duì)于細(xì)胞表達(dá)系統(tǒng)可能帶來(lái)的病毒污染問(wèn)題世界各國(guó)均十分重視,ICH Q5A中規(guī)定了相應(yīng)的技術(shù)要求(ICH關(guān)于“生物技術(shù)產(chǎn)品的病毒安全性評(píng)價(jià)”)。綜合以上因素對(duì)于病毒因子的檢查應(yīng)該盡量充分全面。內(nèi)外源病毒的檢定應(yīng)充分考慮細(xì)胞的特性,傳代歷史,培養(yǎng)過(guò)程等因素。例如:
作為單克隆抗體等生物制劑最常用的生產(chǎn)用細(xì)胞系,中國(guó)倉(cāng)鼠卵巢細(xì)胞(CHO)和小鼠NS0和Sp2/0等細(xì)胞系,由于其細(xì)胞來(lái)源的供體或細(xì)胞取材的原因,需要關(guān)注其特定種屬(鼠源)病毒的檢查。
對(duì)于細(xì)胞建庫(kù)過(guò)程中使用過(guò)動(dòng)物來(lái)源的原料:如牛血清,或胰蛋白酶(豬),還需對(duì)特定的動(dòng)物來(lái)源的病毒進(jìn)行檢定。

另外,2015版《中國(guó)藥典》三部的主要變化還有,新增了“人用重組DNA蛋白制品總論”和“單克隆抗體類生物治療藥物總論”這兩個(gè)總論的制定為生物制品藥物的研發(fā)和質(zhì)量控制提供了通用的指導(dǎo)原則。其中“人用重組DNA蛋白制品總論”對(duì)于連續(xù)培養(yǎng)的生產(chǎn)方式,要求應(yīng)對(duì)收獲階段的微生物污染進(jìn)行常規(guī)檢測(cè);“單克隆抗體類生物治療藥物總論”則提出:細(xì)胞培養(yǎng)和收獲可采用限定細(xì)胞傳代,單次收獲產(chǎn)物的方式;也可采用限定細(xì)胞傳代時(shí)間,連續(xù)傳代多次收獲的方式。而對(duì)于兩種方式的收獲階段都有相關(guān)的規(guī)定,每次收獲后均應(yīng)檢測(cè)抗體含量,細(xì)菌內(nèi)毒素及支原體。對(duì)于限定細(xì)胞傳代次數(shù)的生產(chǎn)方式,需要采用適當(dāng)?shù)捏w外方法,對(duì)3次收獲物進(jìn)行外源病毒的檢測(cè)。
文章由珈創(chuàng)生物前沿技術(shù)研究院提供